
本邦において前立腺癌や乳癌は年々増加傾向にあり、最新の統計解析ではいずれの癌も上位3位以内の罹患率になると推計されています。前立腺癌や乳癌は性ホルモン反応性を示し、内分泌治療が有用な治療法として確立していますが、内分泌治療後に発生する性ホルモン不応性癌は、様々な治療に抵抗性を示し、治療成績の改善を阻んでいる状態です。この内分泌治療抵抗性獲得の機序については、性ホルモンレセプターを中心として様々な研究が行われてきましたが、未だに明確なことは分かっていません。癌の治療抵抗性獲得の機序を解明することが非常に重要で、新たな治療戦略の開発に引いては治療成績の改善に繋がることが期待されます。
我々は性ホルモン反応性癌細胞株を用いた実験や内分泌治療後に摘出された前立腺癌検体を用いた解析から、性ホルモン反応性癌細胞では性ホルモン除去によりRho活性化を介した上皮間葉転換(epithelial-mesenchymal transition;EMT)様変化を来すことを見出し報告しました(Prostate. 2012 Jul 1;72(10):1071-9.)。さらに、化学療法後に摘出された乳癌検体においても、治療後に生存した癌細胞において同様のEMT様変化が起こっていることが確認されました(Horm Cancer. 2014 Dec;5(6):414-23.)。以上の結果から、性ホルモン反応性癌細胞は自身に不利な環境下でサバイバルする際にEMT様変化を来すことが推測されます。
一方、性ホルモン依存性癌細胞株や去勢マウスモデルを用いた実験から、性ホルモン除去下では性ホルモン反応性細胞に細胞老化やIL-6等のSASP(senescence associated secretory phenotype)マーカーの発現が誘導されることを見出しました。さらに、内分泌治療後の前立腺癌や化学療法後の乳癌においても類似の反応が見られることを確認しました。現在はEMT様反応と細胞老化等の他の経路との関連性について検討し、癌の治療抵抗性獲得機序についての研究を続けています。
最近報告した研究成果の一部を以下に示します。
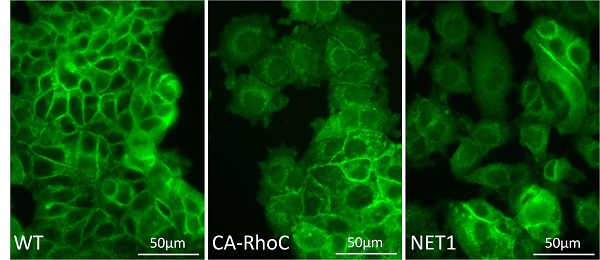
エストロゲン反応性ヒト乳癌細胞株のMCF-7細胞に、活性型のRhoCあるいはRhoを活性化させる因子(Rho-GEF)の一種であるNET1を導入した場合のE-cadherinの発現と形態変化を示します。活性型RhoCあるいはNET1を導入した細胞では、コントロールと比較してE-cadherinの発現低下とともに上皮性の結合が低下していることが分かります。
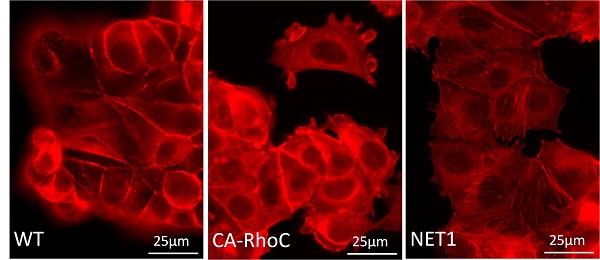
phalloidin染色では活性型RhoCあるいはNET1を導入したMCF-7細胞において、特に上皮性の結合が低下した細胞でActin stress fiber(ASF)の発現が見られ、EMT様変化を来していることが示唆されます。
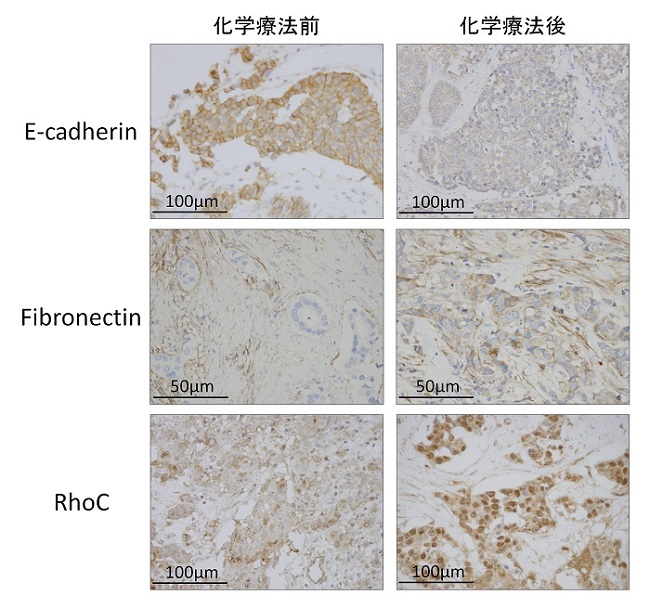
化学療法後に摘出された乳癌の症例において、同一症例の治療前の生検検体と治療後の手術検体とで免疫染色を行い比較しました。治療後にはE-cadherinの発現減弱とともに、fibronectinやRhoCの発現増強が認められました。
 血管平滑筋における胎児型ミオシンを誘導する
血管平滑筋における胎児型ミオシンを誘導するiPS細胞の誘導、心血管・代謝・腎臓等の病態形成に重要
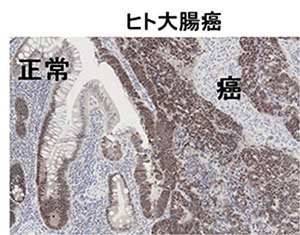
ヒト大腸癌で発現亢進、遺伝子増幅
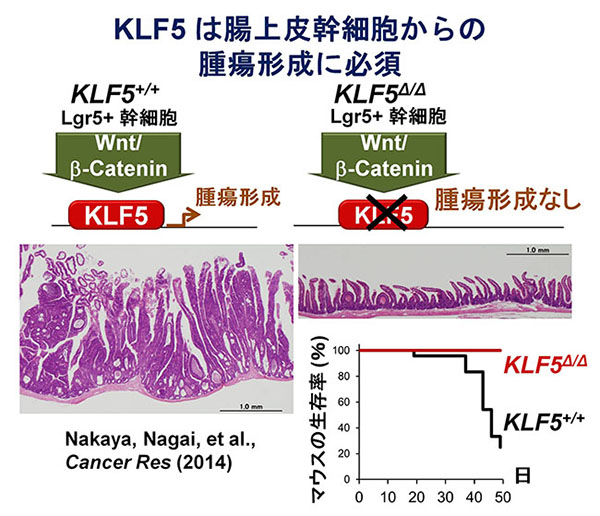
KLF5阻害化合物をもとに、副作用が少なく、癌細胞のみ癌幹細胞から選択的に抑制する、全く新しい大腸癌治療薬の開発を進めます。
さらに、これら化合物がなぜ癌細胞を選択的に抑制するのか分子機構解明を進めます。私たちは、これら化合物が癌細胞では大腸癌を促進する重要因子を抑制するが、正常大腸細胞では抑制しないことを明らかにしています(未発表)。私たちは、癌の分子機構の本質をさらに深く解明し、治療薬の開発と改良にフィードバックし役立てていきます。
日本医療研究開発機構(AMED)「次世代がん医療創生研究事業」に選ばれました。
(研究開発代表者:永井良三 学長)

