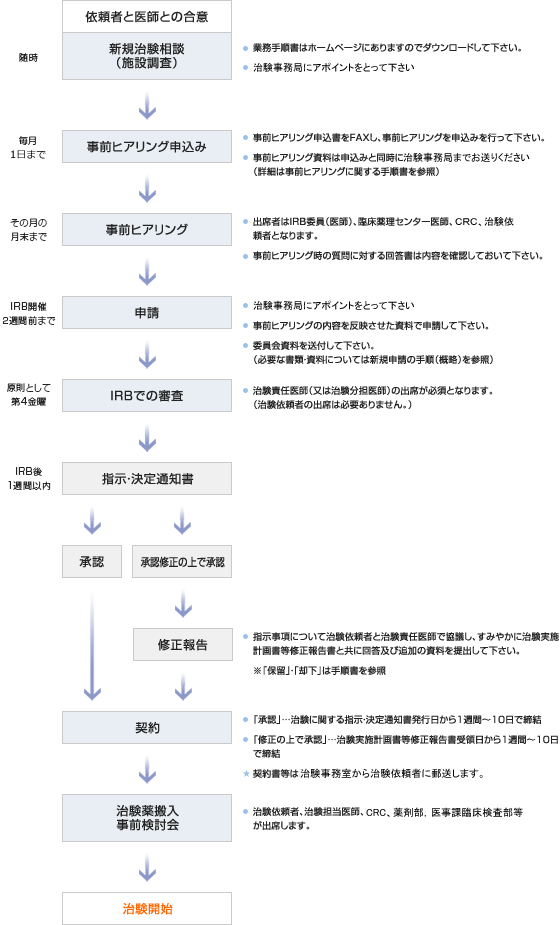
新規申請の概要
《注意》:製造販売後臨床試験においては、「治験」を「製造販売後臨床試験」などに適宜読み替えて準用いたします。
(1)新規治験相談(施設調査)
治験依頼者は、あらかじめ予約を入れ、対面又はMicrosoft Teams等を利用して新規治験相談を行う。
1)予約の受付時間:8時30分~17時15分(平日)
2)電話番号:0285-58-7195(ダイヤルイン)
3)相談対応可能時間:13時30分~17時15分
持参する資料
1)治験実施計画書:2部
2)同意説明文書:1部
3)同意説明文書の電子媒体:1部
4)当日使用する説明用の資料(Power Point等):2部
・後日、電子メールに添付して臨床研究センター(臨床研究・治験推進部)へ送付する。
5)その他、治験依頼者が説明に必要な資料
※治験実施可能性調査・Feasibility調査につきましては、担当医師(治験責任医師候補者等)へ直接ご依頼ください。
(2)事前ヒアリング申込み
- 申込み期間
毎月1日まで - 申込み方法
事前ヒアリング申込書(書式T-21)を臨床研究センター(臨床研究・治験推進部)にメール又はFAXする。
FAX:0285-44-8064
参考資料
- 新規申請に関する手順書
- DDworks Trial Siteを利用
DDTS 利用申請シート(依頼者用)を提出してから、ご利用ください。
DDTS申請マニュアル
Trial Siteシステム化業務フロー - 事前ヒアリング申込書
(3)新規申請
- 新規申請書類等の受付
治験審査委員会開催日の2週間前まで - 申込み方法
DDworks Trial Siteにて交付
(4)新規申請の流れ
《注意》:製造販売後臨床試験においては、「治験」を「製造販売後臨床試験」などに適宜読み替えて準用いたします。